Gezielte MRE Sanierung
Patienten mit einem positiven Keimnachweis müssen unverzüglich dekontaminiert werden. Bei einer gezielten oder vertikalen Dekontamination wird im ersten und wichtigsten Schritt der Fokus auf Keim-Reservoirs über einen Zyklus von 5 Tagen gelegt.
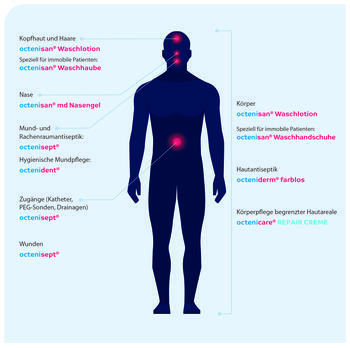
schülke bietet zu diesem Zweck octenidinhaltige Produkte, die ideal miteinander kombinierbar sind. Unsere octenisan®-Range ermöglicht eine sogenannte Bündelstrategie, da keine Wechselwirkungen unterschiedlicher Inhaltsstoffe auftreten können. Das bedeutet für den Patienten höchstmögliche Sicherheit, ganz gleich ob die Dekontamination mit einer Hautdesinfektion mittels octeniderm® farblos, einer postoperativen Wundversorgung mit dem octenilin® Wundgel oder durch eine Wunddesinfektion mit octenisept® geschieht.
Unsere Produkte
Lesen Sie auch
Pflichttexte zu zugelassenen Arzneimitteln gem. § 4 HWG
octenisept®
octenisept®
Lösung zur Wund- und Schleimhautdesinfektion. Zusammensetzung: 100g Lösung enthalten: 0,1g Octenidindihydrochlorid, 2,0g 2-Phenoxyethanol. Anwendungsgebiete: Zur wiederholten, zeitlich begrenzten antiseptischen Behandlung von Schleimhaut und Übergangsepithel vor operativen Eingriffen, - in der Mundhöhle z.B. vor Zahnextraktionen oder Kürettagen, – im Urogenitaltrakt z.B. vor Hysterektomien – und im Rektalbereich z.B. vor dem Veröden von Hämorrhoiden. Im Vulvovaginalbereich mittels Applikator-Sprühkopf bei unkomplizierten bakteriellen Infektionen und Infektionen durch Pilze. Zur zeitlich begrenzten Wund- und Nahtversorgung sowie zur zeitlich begrenzten antiseptischen Behandlung infizierter Wunden der Haut. octenisept® kann bei Erwachsenen und Kindern ohne Altersbegrenzung eingesetzt werden. Die Unbedenklichkeit und Sicherheit der Anwendung ist auch bei Frühgeborenen ab der 24. Schwangerschaftswoche nachgewiesen. Gegenanzeigen: Überempfindlichkeit gegen die Wirkstoffe oder einen der sonstigen Bestandteile. octenisept® sollte nicht zu Spülungen in der Bauchhöhle und der Harnblase und nicht am Trommelfell angewendet werden. Vorsichtsmaßnahmen: Um möglichen Gewebeschädigungen vorzubeugen, darf das Präparat nicht unter Druck ins Gewebe eingebracht bzw. injiziert werden. Bei Wundkavitäten muss ein Abfluss jederzeit gewährleistet sein (z.B. Drainage, Lasche). Hilfsstoffe: (3-Cocosfettsäure-amidopropyl)-dimethylazaniumylacetat, Natrium-D-gluconat, Glycerol 85%, Natriumchlorid, Natriumhydroxid, gereinigtes Wasser. Abgabe: rezeptfrei, apothekenpflichtig. Wirkstoffgruppe: Pharmakotherapeutische Gruppe: Antiseptika und Desinfektionsmittel, ATC-Code: D08AJ57; Octenidin, Kombinationen. Zulassungsinhaber: Schülke & Mayr Ges.m.b.H., Seidengasse 9, A-1070 Wien. Stand der Information: 01.2019. Weitere Angaben wie Dosierung und Art der Anwendung, Warnhinweise und Vorsichtsmaßnahmen für die Anwendung, Wechselwirkung mit anderen Arzneimitteln und sonstige Wechselwirkungen, Fertilität, Schwangerschaft und Stillzeit sowie Nebenwirkungen oder Gewöhnungseffekte entnehmen Sie bitte der veröffentlichten Fachinformation.
octeniderm® farblos
octeniderm®
Lösung zur Hautdesinfektion. Zusammensetzung: 100 g Lösung enthalten: 30,0 g 1-Propanol, 45,0 g 2-Propanol, 0,1 g Octenidindihydrochlorid. Anwendungsgebiete: octeniderm® ist ein Antiseptikum zur Hautdesinfektion vor operativen Eingriffen, Katheterisierungen von Blutgefäßen, Blut- und Liquorentnahmen, Injektionen, Punktionen, Exzisionen, Kanülierungen, Biopsien sowie zur zeitlich begrenzten Nahtversorgung und zur zeitlich begrenzten Prävention katheterassoziierter Infektionen. octeniderm® weist eine remanente Wirkung von 48 h auf. Gegenanzeigen: Überempfindlichkeit gegen die Wirkstoffe oder einen der sonstigen Bestandteile. octeniderm® soll aufgrund des hohen Alkoholanteils nicht bei Frühgeborenen und Neugeborenen mit unreifer Haut angewendet werden. Abgabe: rezeptfrei, apothekenpflichtig. Wirkstoffgruppe: Pharmakotherapeutische Gruppe: Antiseptika und Desinfektionsmittel, ATC-Code: D08AJ57, Octenidin, Kombinationen. Zulassungsinhaber: Schülke & Mayr Ges.m.b.H., A-1070 Wien, Tel. (+43) 1/523 25 01. Stand der Information: 03.2017. Weitere Angaben wie Dosierung und Art der Anwendung, Warnhinweise und Vorsichtsmaßnahmen für die Anwendung, Wechselwirkung mit anderen Arzneimitteln und sonstige Wechselwirkungen, Fertilität, Schwangerschaft und Stillzeit sowie Nebenwirkungen entnehmen Sie bitte der veröffentlichten Fachinformation.